
다원자 이온이란
다원자 이온이란 둘 이상의 원자들이 공유 결합하여 하나의 이온처럼 알짜 양전하 혹은 음전하를 가지는 이온을 뜻합니다.
좀더 부연하자면, 다원자 이온은 둘 이상의 강하게 공유 결합하고 있는 원자들로 구성되는데, 전자가 많거나 부족하여 양전하나 음전하를 띠는 성질을 갖고 있습니다.
참고로, 다원자 이온은 라디컬 이온(radical ion)이라고도 불리는데, 이처럼 다원자 이온은 화학반응을 할 때 원자로 쪼개어지지 않고 하나의 입자처럼 행동합니다.
다원자이온의 화학식
가령 질산칼륨의 경우, 화학식은 KNO3이며, 각 K+가 한 개의 NO3-와 균형을 이룹니다.

질산칼슘의 경우, Ca2+ 하나와 NO3- 두 개를 포함하므로 Ca(NO3)2가 됩니다.

이들 2개의 화학식에서 다원자 이온에 괄호유무의 차이를 발견할 수 있는데요.
이것은 화학식 단위 안에 같은 다원자 이온이 둘 이상 있는 경우에는 괄호 안에 이온을 적고 밖에 아래 첨자를 써야 하는 규칙이 있기 때문입니다.
그렇기 때문에 질산칼륨의 경우 NO3-가 2개이기 때문에 괄호안에 다원자 이온을 적고 괄호 밖에 이온 개수를 아래 첨자로 기재하였으나, 질산칼슘의 경우, 다원자 이온인 NO3-가 1개이기 때문에 괄호가 필요하지 않습니다.
대표적인 다원자 이온
아래 사진은 대표적인 다원자 이온들의 모음인데, 대부분의 다원자 이온은 주로 비금속인 원소가 하나 이상의 산소 원자와 결합한 산소산 음이온(oxianion)입니다.
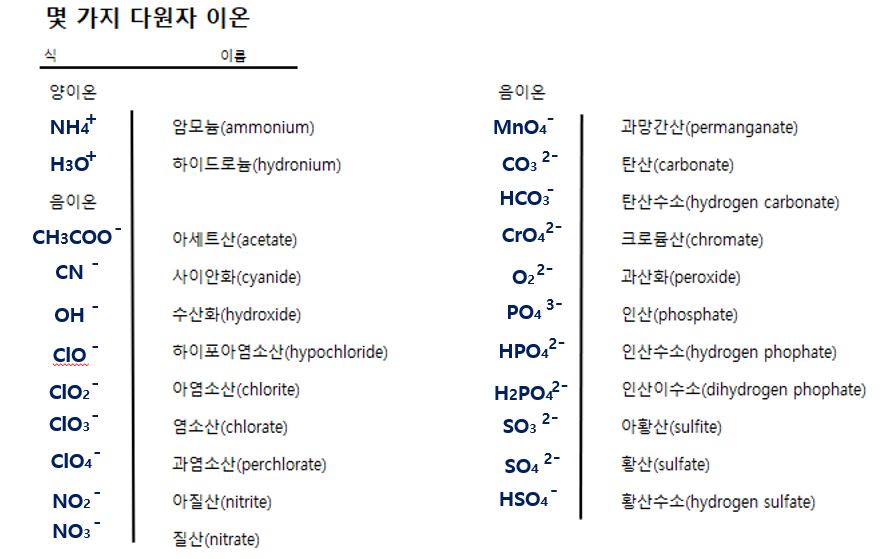
산소산 음이온(산소음이온)의 명칭을 붙이는 규칙은 아래와 같습니다.
1. 가장 많은 산소(O)원자를 가지는 이온은 접두사 과-(영어는 per-), 비금속 어근, 접미사-산(영어는 -ate)을 붙인다.
2. 하나 적은 산소(O)원자를 가지는 이온은 어근에 접미사 -산(영어는 -ate)을 붙인다.
3. 둘 적은 산소(O)원자를 가지는 이온은 어근에 접두사 아-와 접미사 -산(-ite)을 붙인다.
4. 가장 적은(셋 적은) O원자를 가지는 이온은 접두사 하이포아-(영사는 hypo-), 비금속 어근 , 접미사 -산(영어는 -ite)를 붙인다.

글봐주셔서 고맙습니다.
구독,좋아요
한 번씩만 눌러주시면 저에게 큰힘이 되겠습니다.
(비로그인도 구독,좋아요됩니다~ 마음껏 눌러주세요)

'화학 공부' 카테고리의 다른 글
| 일반화학 : 산(Acid)의 명명법(이성분 산과 수소산의 구분) (1) | 2021.10.06 |
|---|---|
| 수화된 이온 결합 화합물 명명법 (0) | 2021.10.06 |
| 화합물 명칭법 - 두 가지 이상의 이온을 가진 화합물의 화학식과 명칭법 (0) | 2021.10.04 |
| 이성분 이온결합 화합물의 화학식과 명칭 붙이는 방법 - 1 (0) | 2021.10.03 |
| 일반 화학 : 화학결합의 종류 - 공유결합 (0) | 2021.09.30 |







